氧化还原反应第一课时学案
1、一、相关知识点的回顾
1.化学反应的分类方法
⑴根据反应物和生成物的类别及反应前后物质种类的多少,把化学反应分为那些类型?
⑵根据反应中物质是否得到氧或失去氧.把化学反应分为?
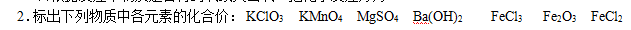
2、二、自主学习内容
1.从化合价升降角度认识氧化还原反应
物质所含元素化合价升高的反应是什么反应?物质所含元素化合价降低的反应是什么反应?
氧化还原反应的概念是什么?

3、【探究活动】从氧化还原反应的角度认识四种基本反应类型,画出四种基本反应类型与氧化还原反应的交叉分类示意图。
2.从电子转移角度理解氧化还原反应的实质
【探究活动】从物质的结构探究氧化还原反应化合价升降的本质
以反应2Na+Cl2 ====2NaCl为例形成离子化合物时,化合价变化的原因是什么?
形成离子化合物时,化合价的变化与电子得失的关系。
以反应H2 + Cl2 == 2HCl 为例形成共价化合物时,化合价变化的原因是什么?
形成共价化合物时,化合价的变化与共用电子对的偏移情况的关系。
氧化还原反应的实质是什么?
4、3. 氧化还原反应中电子转移的表示方法“双线桥法—表示电子转移情况”
【探究活动】如何用双线桥标出氧化还原反应中电子转移的方向和数目。
例:Fe2O3+3CO===2Fe+3CO2
教师提醒:①双线桥箭头从反应物指向生成物连接化合价变化的同种元素;② 线上标明电子得失以及得失的数目③失电子总数=化合价升高总数==得电子总数==化合价降低总数。
用双线桥法分析元素化合价升降,得失电子,被氧化,被还原,氧化反应,还原反应的关系。
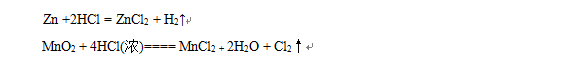
5、【思考交流】1.下列变化过程一定属于还原反应的是
A. HCl→MgCl2 B. Na→Na+
C.CO→CO2 D.Fe3+→Fe2+
6、三、预习中的疑难问题
7、
◇ 自我检测◇
第三节 氧化还原反应⑴
班级 姓名 学号
1.有关氧化还原反应实质的说法中正确的是 ( )
A.有电子的得失或电子对的偏移
B.有元素的化合价的变化
C.有氧元素的参加
D.有原子的重新组合
2.下列有关氧化还原反应的叙述中正确的是 ( )
A.肯定有一种元素被氧化,另一种元素被还原
B.置换反应一定属于氧化还原反应
C.在反应中所有元素的化合价一定发生变化
D.化合反应和复分解反应不可能是氧化还原反应
3.下列反应进行分类时,既属于氧化还原反应又属于化合反应的是 ( )
A.Zn+H2SO4===ZnSO4+H2 ↑ B.CaO+H2O===Ca(OH)2
C.2KClO32KCl+3O2 ↑ D.H2+Cl22HCl
4.下列说法不正确的是 ( )
A.氧化还原反应都是化合反应 B.中和反应都是复分解反应
C.分解反应中的反应物都是一种 D.单质都是同种元素组成的纯净物
5.下列能表示二氧化硫被还原的反应是 ( )
A.SO2+2H2O+Cl2===H2SO4+2HCl B.SO2+H2S===2H2O+3S↓
C.SO2+2NaOH===Na2SO3+H2O D.SO2+Na2CO3===Na2SO3+CO2
6.下列药品置于空气中很容易变质(括号内的物质是变质后的物质),其中不是因为氧化还原反应而变质的是
A.Na2SO3(Na2SO4) B.FeCl2(FeCl3)
C.KI(I2) D.NaOH(Na2CO3)
7.同一物质中同一价态的元素部分被氧化,部分被还原的氧化还原反应是 ( )
A.2HClO===2HCl+O2↑ B.NH4HCO3 NH3 ↑ + CO2↑ +H2O
C.3NO2+H2O===2HNO3+NO D.SO2+2H2S===2H2O+3S↓
8.商代炼铜时,所用的矿物原料主要是孔雀石,主要燃料是木炭,在温度1000℃左右冶炼,可能涉及的反应有:①Cu2(OH)2CO32CuO+CO2↑+H2O②2CuO+C2Cu+CO2↑③CuO+COCu+CO2 ④CO2+C2CO。
⑴从四种基本反应类型来看,①②④的反应类型分别为 , , 。
⑵反应③中, 发生氧化反应, 发生还原反应。
9.已知下列两个反应:①Fe+H2SO4(稀)====FeSO4+H2↑;
②Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O。试回答下列问题:
⑴反应①中 元素被还原,反应②中 元素被还原。(填元素符号)
⑵当反应①生成2g H2时,消耗H2SO4的质量是 g 。
⑶反应②中生成32g SO2气体时,消耗H2SO4的质量是 g ,其中有 g H2SO4作为氧化剂被还原。